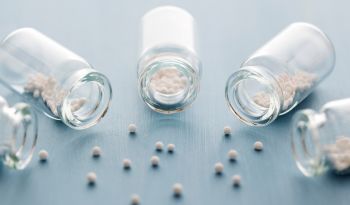
DHEA、睾酮和與年齡相關的認知健康

脫氫表雄酮(DHEA)是睾酮和其它雄性激素的一種前體,在生理機能(如認知調節、食慾和性行為)方面起著重要作用。DHEA以及它的硫形態DHEA-S的血清水平通常會隨著年齡的增長而下降,並在人70歲的時候達到極低水平。血清DHEA水平的逐漸下降造成睾酮合成的減少,而睾酮合成與許多身體症狀、情緒症狀和認知症狀有關,如疲勞、體重下降、情緒低落、易激動、記憶力減退。睾酮對大腦不同部位有益效果的減少造成了這些症狀,因為包括杏仁核和下丘腦在內的大腦部位調節著認知和情緒功能。
動物研究已經發現,外源性DHEA和DHEA-S對抵抗力和心血管系統具有有益的效果。兩種激素原在大腦內還具有神經保護、防氧化和抗炎作用,促進神經生成、增加兒茶酚類神經遞質去甲腎上腺素和多巴胺的合成與釋放。DHEA在西醫中被廣泛使用,以便自我治療與正常年齡增長相關的認知功能衰退。
研究對於DHEA和認知功能有何說法呢?
許多研究已經報告,DHEA可改善健康成年人的工作記憶力、視覺意識、視覺眼肌運動靈敏性和注意力。這些益處可以通過DHEA誘導的皮質重塑來調節,其中皮質重塑可以促進視覺注意的神經過程。但是,關於DHEA對健康成年人以及具有認知障礙的成年人的記憶力的影響,研究結果是不一致的。相對於DHEA水平正常的年輕人,DHEA可能可以改善DHEA血清水平較低的老年人的記憶力。
在一項小型人體試驗(N=10)中,攝入500毫克DHEA的成年男性入睡後快速眼動(REM)睡眠明顯增加。這一發現表明,DHEA引起的大腦內神經類固醇的變化對GABA(γ-氨基丁酸)具有影響。事實上,DHEA與GABA(γ-氨基丁酸)受體和NMDA(天門冬氨酸)受體都有關係,但是,尚不清楚這些受體與DHEA對認知的促進作用是否有密切關係。
一項系統回顧和薈萃分析並未發現DHEA促進健康老年人認知功能的證據。這些發現的意義受到限制,因為只有三項研究符合納入標準,所有被回顧的研究都是為期3個月的研究甚至為期時間更短,並且測試劑量僅在25毫克到50毫克之間。一項獨立的系統回顧和薈萃分析發現,阿茲海默症患者的血清DHEA-S水平皆較低,而DHEA水平正常。作者認為,這一發現符合DHEA在DHEA-S合成中所起的基質作用,作者還認為,阿茲海默症患者在硫酸酯酶的活動或DHEA-S生物轉化的其它分子機制方面可能具有障礙。血清DHEA-S水平的下降可能與阿茲海默症的不同階段或不同嚴重程度有關,比如較低的DHEA-S水平讓認知障礙更為嚴重。需要進一步研究來確定DHEA-S水平是否是診斷阿茲海默症風險的可靠方法。
在一項為期6個月的隨機安慰劑對照研究中,未服藥的男性阿茲海默症患者隨機單獨攝入DHEA(一天兩次,每次50毫克)或安慰劑。3個月後,與一直攝入安慰劑直到研究結束的組別相比,攝入DHEA的組別表現出較好的認知功能。在一項為期4個星期的小型開放研究中,每天通過靜脈注射200毫克DHEA-S的7位多發梗塞性癡呆患者DHEA-S的血清水平和CSF水平明顯提高,在日常活動方面有所改善,並且情緒波動沒那麼頻繁。這兩項研究發現的意義受限於它們的研究規模不大。
老年男性當中低循環的睾酮水平與患阿茲海默症的風險增加相關。在一項為期6個月的安慰劑對照雙盲研究中,16位男性阿茲海默症患者和22位健康成年男性隨機攝入75毫克睾酮(皮膚凝膠形態)和安慰劑以及他們平常使用的藥劑。阿茲海默症患者組別和健康成人對照組別的整體生活質量都得到改善。在研究結束時,兩個組別之間沒有發現明顯區別,但是攝入睾酮的輕度阿茲海默症患者在視覺空間能力方面的退化減少。
DHEA和睾酮的副作用以及安全考量
外源性DHEA和睾酮存在安全性問題。輕度失眠是DHEA不太常見的副作用,所以應該在早上攝入DHEA。若有良性前列腺肥大或前列腺癌的病史,則避免攝入DHEA是明智的做法。睾酮補充劑可能會增加患心血管疾病、中風和前列腺癌的風險。在開始攝入DHEA或睾酮之前,諮詢醫生是明智的做法。
起步不錯,但需要更多研究
需要進行具有前瞻性的大型安慰劑對照研究,以進一步了解DHEA對於健康人士以及阿茲海默症患者或多發梗塞性癡呆患者所具有的可能促進認知的作用,從而確定安全的理想劑量。
References:
- Martínez-Mota, L., Relationship between androgen deficiency and memory impairment in aging and Alzheimer's disease.Actas Esp Psiquiatr, 2017. 45(5): p. 227-47.
- Friess, E., et al., DHEA administration increases rapid eye movement sleep and EEG power in the sigma frequency range.American Journal of Physiology-Endocrinology And Metabolism, 1995. 268(1): p.E107-E113.
- Nguyen, T.-V., et al., Dehydroepiandrosterone impacts working memory by shaping cortico-hippocampal structural covariance during development.Psychoneuroendocrinology, 2017. 86: p. 110-121.
- Evans, JG, et al., Dehydroepiandrosterone (DHEA) supplementation for cognitive function in healthy elderly people.Cochrane Database of Systematic Reviews, 2006(4).
- Pan, X., et al., Dehydroepiandrosterone and dehydroepiandrosterone sulfate in Alzheimer's disease: a systematic review and meta-analysis.Frontiers in aging neuroscience, 2019. 11: p. 61.
- Wolkowitz, OM, et al., DHEA treatment of Alzheimer's disease: a randomized, double-blind, placebo-controlled study.Neurology, 2003. 60(7): p. 1071-1076.
- Azuma, T., et al., The effect of dehydroepiandrosterone sulfate administration to patients with multi-infarct dementia.Journal of the neurological sciences, 1999. 162(1): p. 69-73.
- Lv, W., et al., Low testosterone level and risk of Alzheimer's disease in the elderly men: a systematic review and meta-analysis.Molecular neurobiology, 2016. 53(4): p. 2679-2684.
- Ford, AH, et al., Sex hormones and incident dementia in older men:The health in men study.Psychoneuroendocrinology, 2018. 98: p. 139-147.
- Lu, PH, et al., Effects of testosterone on cognition and mood in male patients with mild Alzheimer disease and healthy elderly men.Archives of neurology, 2006. 63(2): p. 177-185.
- Sheridan, PJ.Androgen receptors in the brain: what are we measuring?Endocr Rev. 1983;4(2):171-8.
免責聲明: 美國食品與藥品管理局並未對上述內容進行評估。本產品不具預防疾病或治療功能,不能取代藥物,不被用於診斷、治療、治癒、支持或緩解任何疾病。


































































 目錄
目錄